I cookie sono piccoli file produtti dal server del sito visitato che vengono scaricati e memorizzati nel disco rigido del computer dell'utente tramite il browser quando lo si visita. I cookie possono essere utilizzati per raccogliere e memorizzare i dati utente durante la navigazione per offrire servizi come il login al sito, una condivisione su social network ecc.. Possono essere essere di natura duratura e rimanere nel pc dell'utente anche dopo la chiusura della sessione dell'utente o svanire dopo la chiusura di essa. I cookie possono del sito che si visita (locali) o di terze parti.
Ci sono diversi tipi di cookie:
- Cookie tecnici che facilitano la navigazione degli utenti e l'utilizzo delle varie opzioni o servizi offerti dal web, come identificare la sessione, consentire l'accesso a determinate aree, facilitano gli ordini, gli acquisti, la compilazione di moduli, la registrazione, sicurezza, facilitando funzionalità (come ad esempio la visione di video ecc...),
- Cookie di profilazione che consentono agli amministratori di tracciare le attività degli utenti e di mandar loro pubblicità mirata,
- cookie di terzi parti che consentono l'integrazione del sito con servizi come i Social Network (cookie sociali) per permetterne la condivisione, cookie flash per la visione di video ecc...
Quindi, quando si accede al nostro sito web, nel rispetto della Direttiva UE 2009/136/CE e del provvedimento 229 dell'8 maggio 2014 del garante della privacy, l'utente ci autorizza all'utilizzo dei Cookie. Tutto questo è per migliorare i nostri servizi. Usiamo Google Analytics per raccogliere informazioni statistiche anonime come il numero di visitatori del nostro sito. I cookie aggiunto da Google Analytics sono disciplinate dalle norme sulla privacy di Google Analytics. Se volete potete disabilitare i cookie di Google Analytics.
Tuttavia, si ricorda che è possibile abilitare, disabilitare, limitare l'utilizzo e cancellare automaticamente i cookies seguendo le istruzioni del tuo browser.
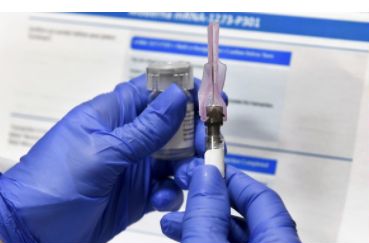 Moderna prevede di richiedere oggi per il suo vaccino contro il coronavirus l’autorizzazione all’uso di emergenza (Eua) all’Fda statunitense (Food and drug administration). La società americana, inoltre, prevede di richiedere oggi anche un’autorizzazione all’immissione in commercio condizionata all’Agenzia Europea per i Medicinali (Ema).
Moderna prevede di richiedere oggi per il suo vaccino contro il coronavirus l’autorizzazione all’uso di emergenza (Eua) all’Fda statunitense (Food and drug administration). La società americana, inoltre, prevede di richiedere oggi anche un’autorizzazione all’immissione in commercio condizionata all’Agenzia Europea per i Medicinali (Ema).



